İYONİK ve KOVALENT BAĞ
İYONİK ve KOVALENT BAĞ
Atomları bir arada tutan kuvvete kimyasal bağ
denir. Atomlar kimyasal bağ yaparken son katmanlarındaki elektron
dizilişlerini soygazlara benzetmeye çalışırlar. Kimyasal bağlar iyonik
ve kovalent bağ olmak üzere ikiye ayrılır.
1. İyonik Bağ: Metal
atomları ile ametal atomları arasında elektron alış verişi ile
gerçekleşen kimyasal bağa denir. İyonik bağ da metaller elektron vererek
+ yüklü iyon (katyon), ametaller ise elektron alarak - yüklü iyon
(anyon) oluştururlar.
Aşağıdaki
örnekte magnezyum atomu son katmanında sahip olduğu 2 elektronunu iki
tane flor atomuna birer tane vererek soygaza benzemektedir. Flor
atomları da soygaza benzemek için eksik olan bir elektronu aldıklarından
onlarda kararlı hale geçer.

Aşağıdaki bir başka örnekte
ise sodyum atomu bir elektron verirken klor atomu bu elektronu alarak
iyonik bağın gerçekleşmesine neden olurlar.

2. Kovalent Bağ: Ametal atomları arasında elektronları ortaklaşa kullanmaları sonucunda oluşan kimyasal bağa denir. Kovalent bağ da ametal atomları kararlı hale geçmek (soygaza benzemek) için eksik olan elektronlarını birlikte kullanarak bu bağın gerçekleşmesine neden olurlar.
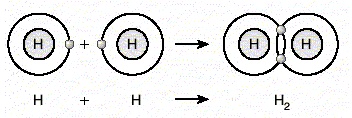
Aşağıdaki örnekte kararsız olan iki tane hidrojen atomu soygaza benzemek için sahip oldukları birer tane elektronu ortaklaşa kullanarak kararlı hale geçerler ve hidrojen molekülünü oluştururlar.
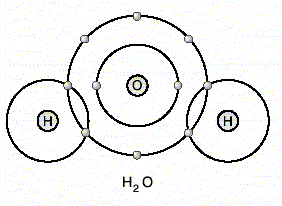
Diğer örneğe baktığımızda ise
oksijen atomu kararlı yapıya ulaşmak için ihtiyacı olan iki elektronu
her birinden birer tane ortak kullanmak koşuluyla iki tane hidrojen
atomundan karşılamıştır. Bunun sonucunda da su molekülü oluşmuştur.






0 yorum:
Yorum Gönder